نانوکریستال های دارویی
نانوکریستال های دارویی
امروزه بسیاری از داروها به دلیل انحلال کم در حلال های مایی و غیر مایی، در مراحل اولیهی تحقیقات کنار گذاشته می شوند. یک راه مناسب برای رفع این مشکل استفاده از نانوکریستال ها است که قابلیت استفاده در صنعت و آزمایشگاه را دارند. برای تولید این ساختارها روشهایی مانند بکارگیری هموژنایزر با فشار بالا یا استفاده از سایش و همچنین روش رسوبی وجود دارد. این ساختارها تاکنون توانستهاند به خوبی جایگاه خود را در بازار و تحقیقات دارویی پیدا کنند و نمونه های موفقی از فرمولاسیون را در سطح دنیا معرفی نمایند. ساده تر بودن ساخت و نیز عوارض کمتر از ویژگیهای اصلی این نانوساختارها است که دلیل عمده ی آن، عدم نیاز به فرمولاسیون های پیچیده برای وارد کردن دارو در ساختار نانو و حفظ پایداری محصول می باشد.
در طی دهه های گذشته با کمک شیمی
و کامپیوتر طراحی های زیادی برای ساختارهای دارویی انجام شده است هر چند، حدود
60% از این ساختارها در آب کم محلول هستند. فرموله کردن این ساختارها از مشکلات
اساسی محققان داروسازی است زیرا این دسته از ترکیبات، به دلیل سرعت انحلال و پخش
شدن آهسته، فراهمی زیستی و جذب کمی خواهند داشت [1]. برای جذب خوراکی، داروها باید
بتوانند شیب غلظتی مناسبی را بین محیط گوارشی و جریان خون ایجاد نمایند. اما در
مورد داروهای کم محلول این شیب غلظتی اندک و در نتیجه جذب نیز کم می شود. در راه
های غیر خوراکی نیز، اگر دارو کم محلول باشد به خوبی در محل تزریق حل نمی شود و
در نتیجه نمی توان سطح مناسبی از دارو را در خون ایجاد نمود. برای رفع این مشکلات
راه حلهایی نظیر استفاده از کمکحلالها، ایجاد نمک، داخل کردن به
سیکلودکسترینها (ساختارهایی شبیه به سبد با حفرهای در وسط که قابلیت ورود
ترکیبات به درون این حفره وجود دارد) یا استفاده از حاملها نظیر لیپوزومها و
پراکندگی جامدات ارائه شده است [1].
متاسفانه استفاده از این راهکارها برای همهی داروها امکانپذیر نیست مثلا برخی
داروها به سختی به یون تبدیل میشوند تا بتوان از آنها نمک ایجاد نمود یا برای
داخل شدن به ساختار سیکلودکسترینها مناسب نیستند. همچنین افزودنیهایی که در
فرمولاسیونها استفاده میشود همیشه کمککننده نیست. به طور مثال محلول دارویی
تزریقی تاکسول که هماکنون در بازار دارویی وجود دارد حاوی مقادیر بالایی از Cremophor EL است که برای بهبود فراهمی زیستی پاکلیتاکسول استفاده شده است اما
موجب عوارض جانبی نظیر شوک آلرژیک میگردد [1].
در دههی 90 میلادی، نانوکریستالهای دارویی توجه محققین دارویی را به خود جلب
نمود. نانوکریستالهای دارویی، پراکندگی کلوئیدی با اندازهی کمتر از میکرومتر
هستند که تقریبا حاوی 100% مادهی فعال دارویی بوده و با کمک مقادیر ناچیز از
پایدارکنندههایی نظیر پلیمرها یا سورفاکتانتها پایدار میشوند [1].
محیط پراکنده کنندهی این ساختارها میتواند آب، محلولهای مایی یا غیر مایی (مثل
پلی اتیلن گلیکول مایع یا روغنها) باشد [2].
بسته به تکنولوژی ساخت، ذرات جامد ایجاد شده میتوانند آمورف یا کریستالی باشند که
در نتیجه به این ذرات، نانوکریستال در ساختار آمورف نیز گفته میشود [2].
2- مزایای نانوکریستالها
• افزایش سرعت انحلال
با کاهش اندازهی ذره سطح تماس بین ذره و محیط اطراف افزایش یافته و در نتیجه سرعت
انحلال (که به میزان سطح تماس مرتبط است) افزایش مییابد (شکل 1) [2].
 شکل 1- با کاهش
اندازهی ذرات سطح تماس افزایش مییابد [2]
شکل 1- با کاهش
اندازهی ذرات سطح تماس افزایش مییابد [2]
• احتمال ایجاد ساختارهای آمورف و مزایای آن
ساختارهای
آمورف سرعت انحلال بیشتری دارند در نتیجه اگر حین تولید این ساختارها ایجاد شوند
زمان مورد نیاز برای انحلال کمتر شده و سرعت اثر دارو افزایش مییابد [2].
• بهبود ویژگیهای زیستی
همانطور که در مقالات قبل نیز ذکر شده است، نانوذرات نسبت به ذرات بزرگتر از نظر
جذب و اثربخشی بهتر عمل میکنند [1].
3- روشهای تهیهی نانوذرات کریستالی
در کل روشهای تولید نانوذرات کریستالی به دو دستهی بالا- پایین (top-down) و پایین- بالا (down-top) تقسیم میشوند. روش پایین- بالا مانند روش رسوبی به این معنا است
که نانوکریستالها از مولکولها ساخته میشوند اما در روش بالا- پایین مانند تکنیک
هموژنایز کردن و سایش دانهای، نانوکریستالها با تخریب و واپاشی مرحله به مرحله
از پودر سخت ایجاد میگردند [1].
3-1- تکنولوژی رسوبی (Precipitation technique)
داروی کممحلول در آب، در یک حلال
(غالبا حلال آلی) حل و محلول به یک ضد حلال (antisolvent) قابل امتزاج با آب (حلال مایی)
افزوده و چرخیده میشود (شکل 2). با این کار اشباع سریع رخ داده و موجب هستهزایی
و ایجاد رسوب میگردد. روش رسوبی این مزیت را دارد که یک داروی خاص میتواند در
حلالهای مختلف، میزان انحلالهای متفاوتی داشته باشد که این امر خود بر هستهزایی
موثر است. هرچند ذرات ایجاد شده در فرمولاسیون نهایی میتوانند رشد کنند و با
افزایش اندازه، موجب بروز مشکلاتی در فراوردههای دارویی شوند. برای جلوگیری از
این پدیده اغلب پایدارکنندهها به فرمولاسیون افزوده میشوند [2و1].
در روش رسوبی، برخی از عوامل بر اندازه و یکسانسازی ذرات اثرگذار است:
سرعت چرخش
نسبت حلال به ضد حلال
مقدار دارو
دما
با افزایش سرعت چرخش، ذرات کوچکتر میشوند زیرا سرعت بالاتر، پخش شدن دارو را بین
فازها افزایش داده و موجب ازدیاد تعداد هستههای ایجاد شده و در نتیجه تولید ذرات
کوچکتر میگردد [2].
اگر نسبت ضد حلال به حلال نیز افزایش یابد موجب اشباعپذیری بین سطوح فازها و
هستهزایی سریعتر میشود [2].
میزان داروی وارد شده نیز نباید زیاد باشد زیرا موجب افزایش احتمال تجمع ذرات اطراف
هم و بزرگتر شدن آنها میگردد.
در این روش معمولا دما را نیز پایین در نظر میگیرند. در دمای پایینتر
اشباعپذیری سریعتر انجام میشود به¬علاوه، با توجه به گرمازا بودن واکنش هستهزایی، هرچه دما کمتر باشد
هستهزایی بهتر انجام میشود [1].
روش رسوبی ساده و مقرون به صرفه است و نیاز به تجهیزات گرانقیمت ندارد. به¬علاوه به دلیل عدم
نیاز به انرژی بالا برای انجام آن، احتمال تخریب دارو نیز کاهش مییابد.
گاه با استفاده از این روش، اشکال آمورف نیز ایجاد میشود که موجب افزایش سرعت انحلال
دارو میگردد. اشکال آمورف یک عیب دارند و آن این است که حالتهای آمورف با انرژی
بالاتر تمایل دارند به فرم کریستاله که پایدارتر است برسند و این مورد بر پایداری
دارو موثر خواهد بود [1].
باقی ماندن حلال در محصول نهایی و نیاز به محلول بودن دارو در حداقل یک حلال، از
دیگر محدودیتهای این روش برای تولید نانوذرات کریستالی است [3].
3-2- روش سایش دانهای (Pearl milling technique)
در این روش دارو، سورفاکتانت و آب وارد محفظه ی سایش حاوی دانه های سایشی
(milling pearls) که از جنس شیشه، زیرکونیوم اکسید یا رزین پلی استایرن هستند شده و
با چرخش دانه ها با انرژی بالا، دارو به نانوذره تبدیل میشود (شکل 3). در کل،
بهینه سازی این روش به عوامل زیر بستگی دارد:
میزان دارو
تعداد دانه های سایشی
سرعت سایش
زمان سایش
دما [2]
اگر میزان دارو و زمان سایش زیاد باشد، احتمال تجمع ذرات و کلوخه شدن آنها افزایش
مییابد. با افزایش سرعت سایش و نیز تعداد دانه های سایشی، میزان انرژی مصرفی
توسط دستگاه بیشتر میشود که از نظر اقتصادی مقرون به صرفه نیست.
در برخی گزارشها ذکر شده است که کاهش دما از کلوخه شدن ذرات جلوگیری مینماید. به
همین دلیل در بسیاری از فرآیندهای تولید، با وارد کردن نیتروژن مایع دمای محفظه ی
سایش را کاهش میدهند [2و1].
روش سایش دانهای ساده است و برای داروهای نامحلول در محیط مایی و غیر مایی کاربرد
دارد. این فرآیند در حجم های مختلف از میلی لیتر تا لیتر قابل استفاده است و در
نتیجه هم در آزمایشگاه های تحقیقاتی و هم در صنعت قابلیت اجرا دارد [2].
اولین محصولی که با این روش تولید شد، Rapamune® بوده است که در سال 2000 معرفی گردید. این روش تولید در مقایسه با
تکنیک رسوبی نیاز به انرژی بیشتری دارد. به علاوه این نگرانی نیز وجود دارد که با
سایش دانه ها ترکیباتی از آنها وارد محصول شده و موجب آلودگی محصول نهایی شود.
همچنین این روش زمانبر است و این زمان ممکن است از چند ساعت تا چند روز ادامه یابد
که همین موضوع احتمال آلودگی میکروبی فرآورده را افزایش می دهد [1].
3-3- روش هموژنایز
کردن با فشار بالا
(High-pressure
homogenization technique)
در این روش، سوسپانسیونی حاوی دارو، سورفاکتانت و آب از یک شکاف بسیار باریک با
سرعت بسیار بالا عبور کرده و ذرات را به اندازهی نانو در میآورد (شکل 4). این
روش نیز مانند روش سایش دانهای، برای داروهای نامحلول در محیط مایی و غیر مایی
مناسب است [2و1].
عوامل زیر بر
بهینه عمل کردن این روش موثر هستند:
سختی ترکیبات وارد شده
فشار اعمال شده
تعداد دفعات
هموژنایز کردن
دما
با افزایش فشار اعمال شده معمولا
اندازهی ذرات کاهش مییابد. اغلب در آزمایشگاهها حداکثر فشار لازم برای تهیهی
نانوذرات کریستالی دارویی حدود 1500 بار است. البته هر چه ذرات سختتر باشند فشار
لازم برای کاهش اندازهی آنها بیشتر خواهد بود [2].
هرچه تعداد دفعات هموژنایز کردن بیشتر شود، ذرات اندازهی یکسانتری خواهند داشت.
با کمک شکل 5 این موضوع روشنتر خواهد شد. طی یک تحقیق اثر تعداد دفعات هموژنایز
کردن بر اندازهی ذرات بررسی شد و نشان داد که با افزایش تعداد دفعات قطر کلی ذرات
به هم نزدیکتر شده و گستردگی اندازهی ذرات که یکی از معایب تولید است، کاهش
مییابد [3و1].
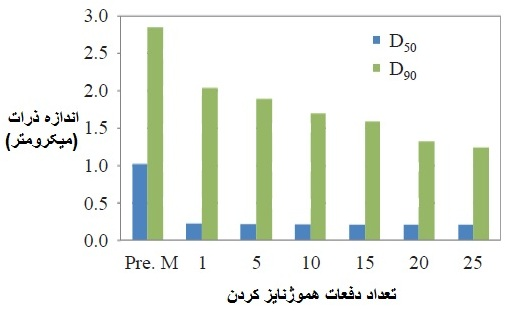 شکل 5- D50 و D90 بهترتیب نشان دهندهی قطر متوسط 50% و 90% از محصولات است. با
افزایش تعداد دفعات هموژنایز کردن، قطر متوسط عمدهی ذرات به هم نزدیکتر میشود
[3].
شکل 5- D50 و D90 بهترتیب نشان دهندهی قطر متوسط 50% و 90% از محصولات است. با
افزایش تعداد دفعات هموژنایز کردن، قطر متوسط عمدهی ذرات به هم نزدیکتر میشود
[3].
با انجام عمل
هموژنایز کردن دمای محفظهی انجام فرآیند افزایش مییابد که برای داروهای حساس به
حرارت مناسب نیست در نتیجه اغلب از یک دستگاه خنک کننده در این روش استفاده میشود
[1].
یک مزیت عمده در این روش قابلیت تولید زیاد محصول بدون نگرانی از آلوده شدن آن است
که نسبت به روش سایش دانهای یک مزیت بزرگ محسوب میشود [1].
جدول 1- مقایسهی دو روش هموژنایز کردن و سایش دانهای [3]
|
روش |
مزایا |
معایب |
|
هموژنایز کردن با فشار بالا |
|
|
|
سایش دانهای |
|
زمانبر بودن |
4- نسل دوم نانوکریستالها
محصولاتی را که با بکارگیری
روشهایی که تاکنون نام برده شد تولید میشوند، نسل اول نانوکریستالها گویند. در
نسل دوم از مخلوطی از روشها برای تولید استفاده میشود. اصل این روشها بر پایهی
هموژنایز کردن است با این تفاوت که پیش از ورود ذرات به هموژنایزر یکسری عملیات بر
روی آنها صورت میگیرد [5و3]. جدول زیر به طور خلاصه نام فرآیندهای نسل دوم و
پیشعملیات لازم بر روی ذرات قبل از مرحلهی هموژنایز کردن را نشان میدهد.
جدول 2- نسل دوم نانوکریستالها [3]
|
فرآیند |
پیش عملیات |
عملیات اصلی |
|
Nanopure |
پیش عملیات لازم نیست اما دارو را در محیط های مایی وارد کرده و سپس هموژنایز میکنند. |
هموژنایز کردن با فشار بالا |
|
H42 |
خشک کردن افشانهای |
هموژنایز کردن با فشار بالا |
|
H69 |
رسوب دادن |
هموژنایز کردن با فشار بالا |
|
H96 |
لیوفیلیزه کردن |
هموژنایز کردن با فشار بالا |
|
CT |
سایش دانهای |
هموژنایز کردن با فشار بالا |
4-1- مزیتهای نسل دوم نانوکریستالها
• نانوکریستالهای کوچکتر
در نسل اول اغلب ذرات ایجاد شده اندازهای کمتر از 200 نانومتر دارند اما در نسل دوم
این محدوده کوچکتر شده و به زیر 100 نانومتر میرسد [5].
• افزایش پایداری فیزیکی
با همراهی روشهایی نظیر سایش و هموژنایز کردن در نسل دوم نانوکریستالها، در
حقیقت از دو راه اندازهی ذرات کاهش مییابد که این امر به کم شدن گسترهی
اندازهی ذرات کمک میکند. هرچه ذرات اندازهی مشابهتری داشته باشند احتمال تجمع
و کلوخه شدن آنها کاهش مییابد که این امر خود از مزایای نسل دوم نسبت به نسل اول
است [5].
5- داروهای وارد شده به بازار
جدول زیر داروهای نانوکریستالی را که تاکنون با موفقیت وارد بازار شدهاند، نشان
میدهد:
جدول 3- داروهای نانوکریستالی وارد شده به بازار دارویی دنیا [3]
|
نام تجاری |
شرکت سازنده |
زمان پذیرش و ورود به بازار |
روش ساخت |
|
® Rapamune |
Wyeth |
آگوست 2000 |
سایش |
|
® Emend |
Merck |
مارس 2003 |
سایش |
|
® TriCor |
Abbott |
نوامبر 2004 |
سایش |
|
®Megace |
Par Pharmaceutical |
جولای 2005 |
سایش |
|
®Triglide |
Skye Pharma |
می 2005 |
هموژنایز کردن با فشار بالا |
®Rapamune حاوی داروی سیرولیموس
است که به عنوان سرکوبکنندهی ایمنی بکار میرود. این دارو به دو صورت سوسپانسیون
خوراکی و قرص در بازار وجود دارد که البته قرصها 21% فراهمی زیستی بالاتری دارند
[2].
® Emendحاوی داروی Aprepitant است که یک ضد تهوع میباشد. این دارو برخلاف اغلب داروهای ضد تهوع
در شیمیدرمانی که به صورت تزریقی مصرف میشوند، به صورت قرص بوده و همین امر یک
مزیت عمده محسوب میشود که باعث بیشتر شدن همراهی بیمار میگردد [2].
® TriCorحاوی داروی Fenofibrate است. اثر دارو بسته به
آنکه بیمار دارو را با معدهی پر یا خالی مصرف کند متفاوت است. هنگام پر بودن معده
انحلال افزایش یافته و جذب بیشتر میشود. با کاهش اندازهی این دارو به نانوذرات،
حلالیت دارو افزایش مییابد و دیگر تفاوتی بین خالی یا پر بودن معدهی بیمار وجود
ندارد. فرمولاسیون دیگر حاوی این دارو که به صورت نانوکریستال است ®Triglide نام دارد [2].
محصول دیگر ®Megace است که حاوی داروی Megestrol میباشد. مزیت این فرمولاسیون که به صورت پودر است، راحتتر بودن
بلع توسط بیمار به علت کاهش گرانروی دارو در فرم نانو و نیز کمتر بودن حجم داروی
مصرفی میباشد [2].
داروهای دیگری نیز به صورت نانوکریستال وجود دارند که در حال گذراندن مراحل بالینی
برای ورود به بازار دارویی هستند. نام این داروها در جدول 4 ذکر شده است.
|
نام تجاری |
دارو |
مورد مصرف |
شرکت سازنده |
مرحله ی بالینی |
|
Semapimod |
Guanylhydrazone |
مهارکنندهی آلفا TNF |
Cytokine Pharma science |
فاز II |
|
Paxceed |
Paclitaxel |
ضد التهاب |
Angiotech |
فاز III |
|
Theralux |
Thymectacin |
ضد سرطان |
Celmed |
فاز II |
|
Nucryst |
Silver |
ضد باکتری |
Nucryst Pharmaceutical |
فاز II |
6- محدودیتهای نانوکریستالها
نانوذرات با اندازههای کمتر از 150 نانومتر احتمال سمیت سلولی را افزایش میدهند
زیرا این ساختارها توانایی ورود به همه ی سلولهای بدن و ایجاد سمیت در آنها را
دارند. به علاوه این روش تولید اغلب برای داروهای دسته II در داروسازی یعنی
داروهایی با انحلال کم و در عین حال قابلیت نفوذ بالا به بافت ها قابل استفاده
است [6].
بحث و نتیجه گیری
نانوکریستالهای دارویی یکی از مهمترین راههای فرمولاسیون برای داروهای کم
محلول است که تاکنون معرفی شده است. این فرمولاسیونها ساده بوده و نیاز به همراهی
ترکیبات دیگر (که خود میتوانند باعث ایجاد عوارض شوند) برای بهینه سازی ندارند.
با توجه به آنکه تعداد داروهای معرفی شده ی کم محلول در حال افزایش است، گمان
میرود که نانوکریستالها بتوانند در آینده جایگاه مناسبی را در بین
فرمولاسیونهای دارویی برای وارد کردن این داروها داشته باشند.
منابـــــع :
· 1.Gao, L., Zhang, D., Chen, M. ‟Drug Nanocrystals for the Formulation of Poorly Soluble Drugs and Its Application as a Potential Drug Delivery System”, Journal of Nanoparticles Research, Vol. 10, pp. 845-862, (2008).
· 2.Junghanns, J., Müller, R. H. ‟Nanocrystal Technology, Drug Delivery and Clinical Applications”, International Journal of Nanomedicine, Vol. 3, pp. 295-309, (2008).
· 3.Che, E., Zheng, X., Sun, C., Chang, D., Jiang, T., Wang, S. ‟Drug Nanocrystals: A State of the Art Formulation Strategy for Preparing the Poorly Water-Soluble Drugs”, Asian Journal of Pharmaceutical Sciences, Vol. 7, pp. 85-95, (2012).
· 4.Aulton, M. E. ‟Pharmaceutics The Science of Dosage Form Design”, UK: Elsevier Science Health Science Division, (2002).
· 5.Keck, C., Kobierski, S., Mauludin, R., Müller, R. H. ‟Second Generation of Drug Nanocrystals for Delivery of Poorly Soluble Drugs: Smartcrystals Technology”, Dosis, Vol. 24, pp. 124-128, (2008).
· 6.Bansal, S., Bansal, M., Kumria, R. ‟Nanocrystals: Current Strategies and Trends”, International Journal of Research in Pharmaceutical and Biomedical Sciences, Vol. 3, pp. 406-419, (2012).


